Paracelso: distintas formas de baile
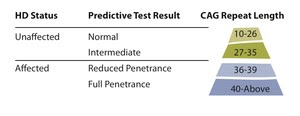
El término “corea” ha sido confuso desde su introducción por Paracelso (1493-1541), en el siglo XVI, hasta nuestros días. Como es sabido, Teofrasto Bombasto von Hohenhan, definió varias formas de “danza” o choreus (de donde derivan palabras como coro, coreógrafo y coreografía): chorea naturalis (refiriéndose quizás a las enfermedades de Sydenham y de Huntington), chorea imaginativa (puede que haciendo referencia a la agitación psicomotora o incluso a los tics) y chorea lasciva (evocando quizás los movimientos pélvicos rítmicos de algunas crisis psicógenas).
Brueghel, el mal de San Vito y la histeria epidémica
Thomas Sydenham, en su Schedula monitoria de novae febris ingressu (Normas de vigilancia de las fiebres que aparecen de nuevo), publicada en 1686,no la relacionó con la fiebre reumática, optando por denominarla “chorea Sancti Viti”. Pretendía evocar con ello,por un lado, el término choreus de Paracelso y, por otro, el famoso grabado de Pieter Brueghel. Es esclarecedor observar con atención la expresiva obra de Brueghel, tantas veces citada, suponiendo que representaba una sorprendente congregación de enfermos huntingtonianos en el día de San Vito
(Fig. 1-1).
Olla podrida
William Osler fue un médico internista que mostró especial interés en el sistema nervioso (escribió 200 artículos sobre temas neurológicos). En su monografía “On chorea and choreiform affections”
(Fig. 1-2), usó el término cervantino de “olla podrida”para significar que el término “corea” se aplicaba a cualquier trastorno del movimiento. En su monografía original, identifica correctamente los coreas de Sydenham y de Huntington, además de las formas “secundarias”. Intentó visitar personalmente a las familias originales de George Huntington, cosa que su médico de familia entonces le desaconsejó “por la enorme sensibilización de los enfermos al respecto”
.

Van Gehuchten, pionero de las sesiones de vídeo
El caso de van Gehuchten, pionero de la Neurología belga y fervoroso defensor de la teoría neuronal de Cajal, es un buen ejemplo del confuso concepto de “corea” hasta bien entrados en el siglo XX. En el libro de Neurología publicado por su hijo en 1920, años después de su fallecimiento, documenta con fotografías un curioso trastorno del movimiento ocurrido casi simultáneamente en once chicas residentes en un orfanato. De acuerdo con su experiencia en otros casos, van Gehuchten clasifica los “coreas histéricos” según su fenomenología; existirían así coreas salutatorios, coreas natatorios y coreas martilleantes. Contemplando las ilustraciones de su libro no es fácil imaginar cómo serían exactamente los movimientos anormales del “corea salutatorio”, la forma observada en sus casos. La singular circunstancia de haber filmado a dos de las muchachas más representativas y que la película sobreviviera milagrosamente alas bombas incendiarias de la Primera Guerra Mundial, demuestra que lo que van Gehuchten interpretó como“corea” correspondía fenomenológicamente a un trastorno del movimiento bien diferente.
La saga de los Huntington
George Huntington, de una típica familia americana de clase media, ejerció, como su padre George H. Lee (n. 1850) y su abuelo Abel (n.1777), como médico rural en East Hampton. George se casó con Mary Elisabeth Hackard, tuvo seis hijos y murió asmático después de una vida dedicada a sus enfermos, a la caza ya la pesca, y también fue aficionado al dibujo
(Fig. 1-3). No puede decirse que fuera la vida de un científico.Tampoco es que su trabajo fuera publicado en una revista de impacto.Ocupaba apenas cuatro páginas ya pareció en 1872, en el Medical and Surgical Reporter, una oscura revista profesional de Ohio. En el borrador del manuscrito,conservado en nuestros días, se observan acotaciones al margen escritas de mano de su abuelo Abel. Tampoco al joven George se le olvidó nunca su primer encuentro con dos mujeres–madre e hija– con la enfermedad.Acompañaba a su padre a caballo en la visita médica cotidiana, cuando aquellas mujeres fueron acercándose.Impresionado por sus incesantes contorsiones, preguntó a su padre. Recibió una respuesta escueta:
that disorder (ese trastorno), el término con el que se conocía en el pueblo la innombrable enfermedad.
Un viaje UK-USA agitado
¿De dónde procedían las familias asentadas en East Hampton? La corea de Huntington sería una “enfermedad made in USA”, pero gestada en Inglaterra. Corría el año 1630 y el puritano alcalde de Bures Saint Mary, Herbert Pelhman, un pequeño pueblo en la frontera entre Suffolk y Essex, junto con tres hombres más, embarcan en el James Winthrop Fleet rumbo a los Estados Unidos. El viaje hasta Salem, Massachusetts, duró tres meses y debió ser agitado. “Incestos, jolgorios, peleas,acusaciones de brujería” escandalizan al ex alcalde y obligan a encarcelar, llegados a tierra, a varios de los peculiares viajeros. En la pequeña población de Bures St. Mary es bien conocida Mary Haste por su proclividad a ofrecer favores sexuales y su conducta disoluta (a lady of easy virtue). Queda embarazada de un tal Welles y sus hijos, Nicholas, Jeffrey y “Wilkie”, emigran a Estados Unidos. Mary Haste tiene otros tres hijos, todos ellos varones, de otra relación. Se apodan Mulefoot (algo así como “los patamula”), los disolutos pasajeros del James Winthrop Fleet, los que se asentarían en Long Island, en la demarcación a la que la saga de los Huntington ofrecerían durante generaciones sus cuidados médicos. Otra interesante cuestión: ¿por qué una publicación tan modesta alcanzó tal difusión? Aparecer en lengua inglesa tuvo influencia, pero no lo explica todo. El artículo de Huntington tuvo la fortuna de ser referenciado en alemán por Kussmaul y por Nothnagel, lo que facilitó grandemente su difusión entre los lectores europeos, en una época de gran interés sobre la eugenesia. Pero fue sin duda el gran William Osler, a la sazón profesor de Medicina en la Universidad McGill de Montreal, el elemento clave en interesarse por el significado de la publicación de Huntington. Estuvo especialmente interesado enlos coreas y, como hemos visto, intentó incluso examinar personalmente a las familias originales de East Hampton.