La enfermedad de Huntington es un trastorno hereditario de
transmisión autosómica dominante, cuyo gen posee una baja penetrancia en la
infancia y juventud, y prácticamente completa (100%) en individuos de 70-80
años.
 Gracias al análisis de numerosas familias americanas
recogido en una amplia base de datos, se ha podido demostrar que los síntomas
de la enfermedad tienden a aparecer en edades más tempranas a medida que
avanzamos en las generaciones siguientes, especialmente si se transmite a
través del padre, fenómeno denominado "anticipación".
Gracias al análisis de numerosas familias americanas
recogido en una amplia base de datos, se ha podido demostrar que los síntomas
de la enfermedad tienden a aparecer en edades más tempranas a medida que
avanzamos en las generaciones siguientes, especialmente si se transmite a
través del padre, fenómeno denominado "anticipación".
La localización del gen es concreta, en el brazo corto del
cromosoma 4. El exón 1 de este gen, llamado IT15, contiene una secuencia
repetida de tripletes CAG, responsable directo de la enfermedad.
El gen IT15, de 200 kb de longitud, contiene en total 67
exones de los cuales el número 1, como hemos dicho antes, contiene una
secuencia repetida de tripletes CAG muy polimórfica. Su tamaño varía entre 10 y
35 repeticiones en la población general, siendo los alelos más frecuentes
aquellos que contienen entre 15 y 20 CAG. En los pacientes con enfermedad de
Huntington, la longitud de esta secuencia está expandida, conteniendo 36 o más
repeticiones. Las mutaciones por amplificación de una secuencia de repetición
polimórfica se denominan mutaciones dinámicas, descritas por primera vez en
1990.
Atendiendo al número de repeticiones CAG del gen IT15
distinguimos tres tipos de alelos :
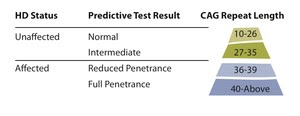
- Normales. Contienen entre 10 y 26 repeticiones
- Intermedios. Contienen entre 27 y 34 repeticiones. Las personas portadoras de estos alelos no desarrollan la enfermedad, pero debido a la inestabilidad de la secuencia CAG, existe un riesgo de que esta se expanda en sus hijos hasta alcanzar el rango patológico. Se denominan alelos mutables.
- Patológicos. Contienen 36 o más repeticiones. Las personas portadoras de estos alelos tienen un riesgo alto de desarrollar los síntomas de la enfermedad de Huntington a lo largo de su vida. Estos alelos patológicos se clasifican a su vez en dos grupos:
- Alelos de baja penetrancia. Contienen entre 36 y 39 repeticiones CAG y sus portadores pueden no desarrollar la enfermedad, aún viviendo hasta la década de los ochenta.
- Alelos de penetrancia completa. Contienen 40 o más repeticiones y se asocian a la presencia de manifestaciones clínicas.
El análisis del número de repeticiones CAG nos permite
realizar un diagnóstico directo y seguro de la enfermedad, independientemente
de la presencia o no de los síntomas.
En cuanto a la relación fenotipo-genotipo, el número de
correlaciones CAG está en correlación inversa con la edad de comienzo de los
síntomas de la enfermedad de Huntington. Las personas con una forma adulta de
la enfermedad presentan generalmente tamaños que pueden variar entre los 40 y
los 55 CAG, en tanto que las formas juveniles,frecuentemente, se asocian a
expansiones mayores, superiores a las 60 repeticiones.
 Tanto la enfermedad de Huntington como otras enfermedades de
herencia dominante se expresan en heterocigotos ( personas portadoras de un
alelo mutado y otro normal en el mismo locus). En circunstancias excepcionales
(ambos padres afectados), una persona puede heredar las dos copias mutadas de
un gen dominante. Por lo general, los homocigotos o portadores de doble dosis
de enfermedades dominantes presentan una clínica mucho más grave y muy
frecuentemente son letales. La enfermedad de Huntington es una de las pocas
excepciones a esta regla, ya que los homocigotos son clínicamente semejantes a
los heterocigotos, si bien se sospecha un inicio más temprano de los síntomas.
Tanto la enfermedad de Huntington como otras enfermedades de
herencia dominante se expresan en heterocigotos ( personas portadoras de un
alelo mutado y otro normal en el mismo locus). En circunstancias excepcionales
(ambos padres afectados), una persona puede heredar las dos copias mutadas de
un gen dominante. Por lo general, los homocigotos o portadores de doble dosis
de enfermedades dominantes presentan una clínica mucho más grave y muy
frecuentemente son letales. La enfermedad de Huntington es una de las pocas
excepciones a esta regla, ya que los homocigotos son clínicamente semejantes a
los heterocigotos, si bien se sospecha un inicio más temprano de los síntomas.
Hoy en día se considera que el tamaño de la secuencia CAG
condiciona, aproximadamente, un 50-65 % de la variabilidad en la edad de
comienzo de los síntomas de la enfermedad. Sin embargo, el efecto de esta
secuencia es llamativamente inferior en personar con un número de repeticiones
entre 40 y 50 repeticiones, que en aquellas con 50 o más. Esta circunstancia sugiere que los factores
modificadores, diferentes a la longitud de la secuencia, tienen un mayor
impacto en aquellas personas con expansiones pequeñas, circunstancia que
explicaría la amplia variabilidad en la edad de comienzo de los síntomas que se
observa en pacientes con un número de repeticiones entre 40 y 45.
En relación a la anticipación genética (incremento de la
gravedad o disminución de la edad de comienzo de los síntomas en generaciones
sucesivas ), podemos decir que es un fenómeno predominante en el Huntington y
en otras enfermedades causadas por mutaciones dinámicas. Su efecto depende del
sexo del progenitor. En nuestro caso, la anticipación se produce más
frecuentemente por transmisión del alelo mutado a través de la vía paterna,
como consecuencia de la inestabilidad de la repetición CAG durante la espermatogénesis.
Las expansiones grandes se producen casi exclusivamente a través del padre.
 |
| Cromosoma 4 |
| Gen de la Htt |
Estudios genéticos
- Alelos intermedios
y nuevas mutaciones: Más de un 25-30% de los casos diagnosticados no refieren
antecedentes familiares. El análisis del gen IT15 en estas familias ha
demostrado que gran parte de estos casos esporádicos son consecuencia de la
expansión, hasta el rango patológico, de un alelo intermedio (27-35
repeticiones de CAG) presente en los padres. Estos alelos intermedios se
transmiten preferentemente a través de la línea germinal de los varones y su
inestabilidad se asocia a una edad avanzada paterna, circunstancia previamente
descrita en otras enfermedades dominantes. De esta manera, se explica la
existencia de nuevas mutaciones en el
Huntington, estimándose hoy en día una tasa en torno al 10 %.
- Genes modificadores: La presencia en dos personas de una misma expansión de tripletes CAG en el gen del Huntington no se traduce, ni mucho menos, en la existencia de unas manifestaciones clínicas semejantes. Además del tamaño de la secuencia CAG, el inicio de los síntomas motores depende claramente de la presencia de otros genes y de factores ambientales cuya contribución se estima en un 40 y 60%,respectivamente, de la variabilidad residual.
 E2F2 es un gen que codifica para un factor de transcripción
con implicaciones en el ciclo celular, regulando la fase quiescente de los
linfocitos T y sobre todo (en lo que atañe a esta enfermedad) tiene un
importante papel en la diferenciación de los terminales neuronales.
E2F2 es un gen que codifica para un factor de transcripción
con implicaciones en el ciclo celular, regulando la fase quiescente de los
linfocitos T y sobre todo (en lo que atañe a esta enfermedad) tiene un
importante papel en la diferenciación de los terminales neuronales.
El rs2742976 se localiza en un supuesto sitio de unión
(STATX) en la región promotora del gen E2F2, existiendo una correlación entre
el genotipo rs2742976 y la expresión del gen E2F2, siendo mayor en los
individuos con el polimorfismo TT que los individuos GG. Esto quiere decir que
la presencia del alelo T en el genotipo E2F2 rs2742976 indica una menor
expresión del factor de transcripción E2F2, lo que a su vez está relacionado
con una aparición más tardía de los síntomas propios del Huntington.

No hay comentarios:
Publicar un comentario